Léčebné metody
Jak probíhá léčba na Klinice IVF Zlín?
Léčebné metody
Indukce ovulace je hormonální podpora růstu a dozrávání vajíček ve vaječnících pro následné přirozené oplodnění. Je vhodná především u žen s anovulačními cykly, kde nedochází k pravidelnému uvolňování zralého vajíčka. Pro stimulaci vaječníků používáme rozmanité hormonální léky. Základním a nejčastěji používaným přípravkem je klomifencitrát (Clostilbegyt). Ultrazvukovým vyšetřením se během stimulace sleduje počet a velikost folikulů ve vaječnících, ve kterých se vajíčka vyvíjejí. Hodnotí se taktéž charakter a výška děložní sliznice. Rizika spojená s touto metodou jsou minimální, s výjimkou možnosti vzniku vícečetného těhotenství a případných komplikací s ním spojených.
Minimální stimulace vaječníků je určená pro ženy, které nechtějí podstoupit klasickou stimulaci IVF. Ke stimulaci se využívá tablet Clomiphen citrátu (Clostilbegyt) v kombinací s nízkými dávkami injekčních preparátů, které jsou známé z klasických IVF cyklů. Oplození vajíčekprobíhá metodou ICSI event. PICSI. Pravděpodobnost otěhotnění je nižší než u klasického IVF, ale je nižší riziko OHSS (hyperstimulace) i nižší náklady na stimulaci IVF.
V praxi je nejčastěji minimální stimulace využívána v těchto případech:
- Předchozí stimulace byla komplikovaná ovariálním hyperstimulačním syndromem.
- Žena má obavu z hormonální stimulace vyššími dávkami.
- U žen se syndromem polycystických vaječníků (PCO syndrom).
- U opakovaného selhání léčby neplodnosti metodou klasického IVF.
- Při nutnosti minimalizace nákladů na léčbu.
Jedná se o nejjednodušší metodu asistované reprodukce. Spermie se metodou SWIM UP (vycestování) zkoncentrují a pročistí. Poté se zavádějí speciálním katetrem do dutiny děložní v období ovulace. Jedná se o relativně jednoduchý a bezbolestný výkon, provádí se ambulantně bez anestezie. Tento typ léčby je vhodný při hraničních hodnotách spermiogramu. Úspěšnost IUI po stimulaci vaječníků se pohybuje mezi 10-15 % na cyklus.
Komu je metoda určena
IUI je obvykle určena párům, u kterých snaha otěhotnět i po ročním úsilí nebyla završena úspěchem a u kterých zatím není zcela jasná příčina neplodnosti. Před samotným procesem IUI byste měla projít důkladným vyšetřením příčiny neplodnosti.
Metoda IUI se zakládá na přirozené schopnosti spermií oplodnit vajíčko v pohlavním traktu ženy. Studie dokazují, že tato metoda je neefektivní v případech, kdy sperma partnera má nízkou koncentraci nebo spermie mají špatný tvar.
Ženy s poruchami ovulace se mohou léčit metodou IUI v případě, že jejich reakce na stimulaci je adekvátní. V těchto případech hormonální léčba stimuluje ovulaci a IUI je načasovaná na období ovulace. Hormonální stimulace se obvykle používá i u žen bez poruch ovulace.
Ženy s endometriozou se mohou léčit metodou IUI, když nemají žádné deformace orgánů v břišní dutině. Ženám s neprůchodností vejcovodů metoda IUI nepomůže.
V případech, kdy nelze použít spermie partnera, je možná umělá inseminace spermatem dárce (AID), kdy se použije sperma anonymního vyšetřeného dárce. Naše centrum se řídí zákony a právními předpisy České republiky. Z hlediska těchto nařízení je použití čerstvého spermatu dárce pro inseminaci zakázané. Všechny vzorky spermatu musí být zmraženy a uskladněny po dobu 6 měsíců a dárce se musí opět otestovat na přítomnost infekčních onemocnění. Před tím, než se daný vzorek spermatu poskytne k použití, musí být oba výsledky, při odběru a půl roku po zamražení negativní.
Přínos metody
Úspěšnost metody IUI je od 10 % až do 15 % na cyklus (v závislosti na věku ženy).
Partnerský pár může podstoupit několik cyklů IUI. Pokud nedojde k otěhotnění, lékař zpravidla doporučí účinnější léčebnou metodu – in vitro fertilizaci (IVF).
Výhodou metody IUI je, že nevyžaduje odběr vajíčka a celkovou anestezii.
Postupy:
- Použití hormonálních přípravků stimuluje 2 až 3 vajíčka k dozrání. Ke stimulaci se obvykle používají tabletky Clomiphene citrátu nebo injekce gonadotropinu.
- Monitorování léčby se provádí měřením velikosti folikulů a individuálním přizpůsobení dávky hormonálních přípravků. Cílem IUI je obvykle stimulovat růst a dozrání 1-3 folikulů.
- Když folikuly dosáhnou požadované velikosti, dostanete injekci hCG startující ovulaci.
- V den ovulace partner ráno poskytne sperma, které se připraví k inseminaci. Čerstvé sperma se po odběru a zkapalnění propere a zkoncentruje. Lékař pomocí jemného katetru zavede připravené sperma přes hrdlo až do dělohy. Celý proces je bezbolestný.
První pokus s umělým oplozením byl poprvé úspěšný v roce 1978, kdy se díky lékařům R. Edwarse a P. Steptoea, narodilo první dítě na světě metodou IVF/ET (Louise Brownová – Velká Británie). Ve světě se ročně narodí více než 3,7 milionu dětí, které byly počaty metodami asistované reprodukce. Je to komplex postupů, při kterých se manipuluje přímo se zárodečnými buňkami – vajíčky a spermiemi – mimo organismus ženy – proto mimotělní oplodnění.
Po hormonální přípravě směřující k dozrání většího počtu vajíček, jsou tato těsně před ovulací přenesena odsátím přímo z vaječníků do speciálního kultivačního média spolu s vybranými spermiemi partnera. Po oplození dochází ke kultivaci oplodněných vajíček (embryí) ve speciálních médiích, kdy již fertilizační proces probíhá zcela přirozeně a bez zásahu zvenčí. Embrya jsou pak transferována zpět do dělohy ženy.
Příprava před IVF:
Hormonální stimulace:
Vícenásobný růst vajíček zvyšuje možnost získání většího množství kvalitních vajíček a následně více embryí vhodných pro transfer. Je to dosaženo stimulací ženy hormonálními léky, přičemž žena je neustále pod kontrolou lékaře.
Odběr vajíček:
Odběr vajíček z vaječníků se vykonává v krátkodobé celkové anestezii pod kontrolou transvaginálního ultrazvuku a trvá v průměru 5-10 minut. Výkon je prováděn speciální punkční jehlou, která se přes poševní stěnu dostane až k vaječníku, odkud se následně odsávají vajíčka. Pacientka je po tomto výkonu propuštěna domů asi po 2 hodinách.
Odběr a příprava spermií:
Vzorek spermií se získává od partnera v den odběru vajíček ve speciální zvukově izolované místnosti určené pro tyto účely. 2-5 dní před odběrem spermií je doporučena sexuální abstinence ve snaze získat co nejkvalitnější vzorek spermatu. Po jeho laboratorní úpravě jsou vajíčka oplodněna partnerovými spermiemi ve společném roztoku. K oplodnění dochází spontánně, spermie vlastním pohybem docestují k vajíčku a pronikají jeho obaly. Společná kultivace vajíček a spermií trvá 16-20 hodin. Po této době zjišťuje embryolog úspěšnost fertilizace (oplodnění), která je charakterizována přítomností dvou prvojader a dvou pólových tělísek. V případě, že má muž pochybnosti, zda bude schopen získat sperma v den odběru vajíček, má možnost nechat si je zamrazit (kryokonzervovat) předem. MESA/TESE je také jednou z možnosti získaní spermií při IVF cyklu u mužů, kteří nemají žádné spermie v ejakulátu.
Kultivace embryí:
Embrya se kultivují ve speciálních médiích 2-6 dnů, než jsou zavedena do děložní dutiny. Některá nadbytečná embrya mohou být zamražena a uskladněna pro eventuální pozdější použití.
Embryotransfer (ET):
Je metoda, při které se embrya přenášejí do děložní dutiny pacientky tenkým speciálním katetrem. Embrya jsou zavedena s malým množstvím tekutiny – média. Tento výkon je rychlý, většinou bezbolestný a nevyžaduje anestezii. Počet zavedených embryí závisí hlavně na věku pacientky, počtu předchozích neúspěšných IVF cyklů a přání pacientky. Většinou se přenášejí 1- 2 embrya. Pacientka asi po jedné hodině od ET odchází domů. Za 2 týdny se dostaví na Kliniku k vyšetření těhotenského testu.
Nadstandardní kultivace je laboratorní technika, která podstatně zlepšuje výsledky při dosahování těhotenství technikou IVF a ET. Vajíčka, spermie a následně embrya jsou umístěny do speciálních médií (kultivačních roztoků), které vytvářejí vhodné podmínky pro jejich další vývoj. Kultivační roztoky jsou každý den obměňovány tak, aby byly vytvořeny co nejpřirozenější podmínky pro vyvíjející se embrya.
Kultivace do stádia blastocysty
Použitím speciálních kultivačních roztoků je možno prodloužit dobu kultivace embryí až na 5 či 6 dnů (stádium blastocyty). Výhodou tohoto postupu je možnost výběru nejkvalitnějších embryí pro přenos, čímž se zvyšuje pravděpodobnost otěhotnění. Použití prodloužené kultivace je vhodné zejména při dostatečném počtu oplozených vajíček (obvykle 6 a více). Určení optimálního dne pro přenos embryí je zcela individuální a může se při opakování IVF cyklu lišit.
Nadstandardní technika, při níž je do obalu dvou až čtyřdenního embrya proveden pomocí ostré jehly otvor, kterým pak embryo svévolně obal opustí. Je doporučena provádět u embryí se silným obalem nebo v případech tzv. implantační selhání (v předchozích cyklech se embryo samovolně neimplantovalo).
Zmražení embryí je metoda, kterou lze kryokonzervovat nadbytečná embrya a uchovávat je libovolně dlouhou dobu v tekutém dusíku pro pozdější přenos. Kryokonzervace se používá tehdy, když je k dispozici více kvalitních embryí, která nebyla zavedená v daném cyklu (např. pro riziko vícečetného těhotenství). V případě těžkého ovariálního hyperstimulačního syndromu či nevhodných podmínkách pro transfer (např. jiná akutní nemoc pacientky, nízká sliznice děložní apod.) se zamražují všechna embrya. I přes standardizaci postupů ne všechna embrya proces zmrazení a rozmrazení přežijí v takovém stavu, aby mohla být po rozmrazení transferována.
Úspěšnost transferu zamrazených - rozmrazených embryí (kryoembryotransfer- KET) bývá srovnatelná s přenosem čerstvých embryí. Pro ženu je však výhodou, že nepotřebuje opakovanou hormonální stimulaci a další odběr vajíček. Na základě současného stavu vědomostí není známo zvýšené riziko abnormalit či vrozených vývojových vad po uchování embryí touto metodou.
PGT je diagnostická metoda, která v návaznosti na IVF program umožňuje testovat některé genetické vlastnosti embryí před jejich zavedením do dělohy. Z 5-ti denního nebo 6-ti denního embrya (D3) embrya se šetrně odebere 5-10 buněk a podrobí se genetické analýze. Embrya se v den odběru buněk zamrazí. Ke KET (kryoembryo transferu) se pak připraví embryo s normálním genetickým statusem. Embrya tento zákrok přežívají bez jakékoliv újmy.
Preimplantační genetické testování aneuploidií (PGT-A) umožňuje odhalit především získané nebo dědičné odchylky v počtu nebo struktuře chromozomů. Tyto abnormality bývají často spojovány se spontánním potratem.
Preimplantační genetické testování monogenních onemocnění (PGT-M) dokáže odhalit změny (mutace) jednotlivých genů spojené s konkrétním dědičným onemocněním, které se již v rodině vyskytlo.
Preimplantační genetické testování strukturních chromozomových vad (PGT-SR) dokáže odhalit výskyt translokací chromozomů či jiných strukturních přestaveb.
Metoda PGT je doporučena zejména párům, kde:
- Věk partnerky je vyšší než 35 let a je tak zvýšena pravděpodobnost porodu dítěte s abnormálním počtem chromozomů (např. Downův syndrom).
- Se již vyskytl potrat nebo porod plodu s chromozomální poruchou.
- Dochází k opakovaným neúspěchům v IVF léčbě nebo opakovaným potratům v rané fázi gravidity.
- Byla cytogeneticky zjištěna u jednoho z partnerů přestavba chromozomů. Přesto, že tento jedinec sám není zjevně postižen, tato přestavba může mít za následek tvorbu pohlavních buněk (vajíček nebo spermií) s abnormální genetickou výbavou a předání vady potomkům.
- Se v rodině vyskytuje tzv. choroba vázaná na pohlaví (chorobou jsou postiženi jen jedinci mužského pohlaví, ale geneticky je přenášejí ženy - např. hemofilie).
- Jeden z partnerů prodělal nebo prodělává některé druhy chemoterapie nebo radioterapie.
Preimplantační genetické testování nedokáže plně zaručit výběr embrya, které nemá žádný defekt. Je to dáno principem metody, kdy se dá vyšetřit jen určité spektrum odchylek, kterými jsou embrya daného páru nejvíce ohrožena. Stejně tak nemůže zaručit úspěch IVF programu, tedy implantaci embrya po transferu do dělohy a vznik těhotenství. Nemůže garantovat narození zdravého dítěte. To vše je ovlivňováno velkým množstvím dalších faktorů.
Molekulárně diagnostický text k vyšetření receptivity endometria (stavu děložní sliznice).
Receptiva endometria je stav, kdy je endometrium (děložní sliznice) připraveno na implantaci (zahnízdění) embrya. Tato optimální situace by u každé fertilní ženy měla být mezi 17.-21. dnem.
Běžně se endometrium hodnotí dle ultrazvukového vyšetření, které ukáže jeho výšku a strukturu. ERA test nabízí širší možnosti, jak posoudit sliznici, čímž zvyšuje pravděpodobnost úspěšného otěhotnění.
Vyšetření je vhodné pro ženy s opakovaným selháním implantace embrya.
Test vyšetří 238 genů, které se podílejí na receptivitě endometria. Nejvhodnější dobou k provedení testu je cyklus, který předchází cyklu, ve kterém je plánován embryotransfer.
Lékař může vyhodnotit, zda je v daných dnech endometrium správně vnímavé pro přenos embrya nebo zda je tzv. „okno implantace“ posunuto.
Revoluci v pojetí mužské neplodnosti znamenala v roce 1992 zpráva o prvních těhotenstvích, dosažených po injekci jediné spermie skrz obal (zona pellucida) do vajíčka. Tato metoda pomáhá nespočetnému množství párů, které ještě před lety byly považovány za beznadějné a nucené využít dárcovství spermií.
Metoda "intracytoplasmatická injekce spermií" (ICSI) je náročnou mikromanipulační technikou, kdy je spermie nasáta do velmi tenké a ostré skleněné kapiláry a tato je zavedena do vajíčka přes jeho obal a spermie z této kapiláry je vpíchnuta dovnitř vajíčka.
Indikace pro ICSI jsou neschopnost spermií spontánně oplodnit vajíčko (nízký počet, nízká pohyblivost), imunologické příčiny neplodnosti, selhání oplodnění při klasické metodě IVF, při opakovaných neúspěšných pokusech umělého oplodnění, při vyšším věku, při zisku malého počtu vajíček, při užití kryokonzervovaných spermií, při užití darovaných vajíček aj. Tato metoda má velmi vysokou úspěšnost oplození. Pacientka musí samozřejmě podstoupit běžnou proceduru superovulace a odběru vajíček a partner musí dodat vzorek spermatu. Na základě současných znalostí lze konstatovat, že oplození vajíček takto získanými spermiemi nezvyšuje riziko porodu plodu s vrozenou vývojovou vadou ve srovnání s těhotenstvími po spontánním oplození (2,3 %).
Jde o laboratorní techniku (zdokonalená ICSI), která umožňuje vybrat a vpravit do oocytu pouze zralou spermii a tím zvyšuje úspěšnost léčby neplodnosti. Přirozeně jsou schopny oplodnit vajíčko pouze zralé spermie, které se dokážou specificky navázat na tzv. oocytární komplex, konkrétně na hyaluronan. Nezralé spermie, které nemají hyaluronanový receptor, se na oocytární komplex nenavážou a nejsou schopny oplodnit vajíčko. U zralých spermií byl prokázán výrazně nižší výskyt chromozomálních aberací než u spermií nezralých.
Při běžném použití samotné ICSI metody, jsou spermie vybírány na základě jejich morfologie a motility (pohyblivosti), což neposkytuje záruku, že do vajíčka bude vpravena spermie s optimální genetickou výbavou. PICSI spojuje výhody ICSI (vysoká pravděpodobnost oplození vajíčka) s možností vybrat zralou spermii na základě její schopnosti vázat se na hyaluronanový hydrogel. PICSI napodobuje vazbu zralé spermie na oocytární komplex, což je velmi důležité pro selekci vhodných spermií během přirozené fertilizace. Tuto techniku lze použít za předpokladu, že v ejakulátu je dostatečná koncentrace pohyblivých spermií.
Při své praxi využíváme kultivační média – EmbryoGen + BlastGen - obohacené o cytokiny.
Tato kultivační média obsahují vyšší koncentraci cytokinu (GM-CSF), který se přirozeně vyskytuje v děloze matky při normálním průběhu otěhotnění. Cytokiny v médiích EmbryoGen + BlastGen připravují embryo před implantací, pomáhají navázat dialog mezi matkou a embryem a tím podporují vznik a udržení těhotenství.
Kultivační média EmbryoGen + BlastGen pomohou zejména ženám, které mají problémy s přirozeným otěhotněním a podstupují léčbu IVF. Léčba je prospěšná všem ženám a je vhodná zejména v těchto případech:
- Opakující se samovolný potrat
- Časné potraty
- Nevysvětlitelná neplodnost
Jak ještě více pomoci našim pacientům k početí dítěte?
Klinika reprodukční medicíny a gynekologie Zlín nabízí moderní postupy zvyšující šanci na početí vlastního dítěte.
Kultivační médium EmbryoGlue® od společnosti Vitrolife je speciální médium, určené k přenosu embryí přímo do dělohy. Toto médium obsahuje všechny živiny a zdroje energie, potřebné pro optimální vývoj embryí. Ve vyšší koncentraci obsahuje také látku hyaluronan, která se běžně vyskytuje ve folikulární tekutině ve vejcovodech a v děloze, kde vytváří prostředí se zvýšenou viskozitou.
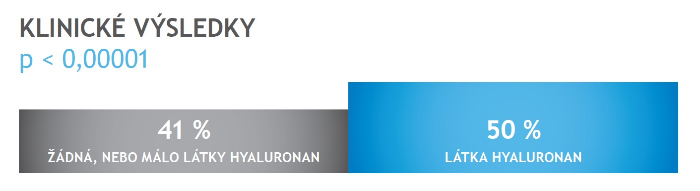
Obr.: Klinické výsledky při použití kultivačního média EmbryoGlue, které obsahuje látku hyaluronan (zdroj: Vitrolife).
Použitím média EmbryoGlue® během přenosu embrya do dělohy (embryotransfer) se tak výrazně zvyšuje šance na otěhotnění, než při použití média bez obsahu hyaluronanu. Kultivační médium EmbryoGlue® je použitelné při embryotransferu všech vývojových stádií embryí, od dvoudenních až po blastocytu a to jak čerstvých, tak zamražených.
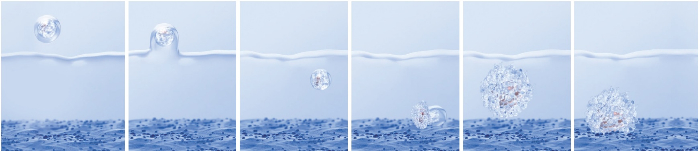
Obr.: Sekvenční průběh embryotransferu při použití kultivačního média EmbryoGlue (zdroj: Vitrolife).
Použití média EmbryoGlue® je nadstanadradní výkon, který není hrazen pojišťovnami.
Žádost o tuto proceduru je třeba hlásit Klinice předem již v době přípravy vlastního cyklu.
Aktuální cenu naleznete v našem ceníku výkonů.
Jedná se o mikrochirurgické odsátí spermií z nadvarlete - zákrok, který se provádí v případě porušení transportu spermií mezi nadvarletem a močovou trubicí. Výkon se až na výjimky provádí v celkovém znecitlivění otevřenou cestou, tj. cca 3 cm dlouhým řezem na šourku se získá přístup k nadvarleti a pipetou se z kanálků odsaje tekutina. Tato je v průběhu operace podrobně analyzována v embryologické laboratoři. Pokud obsahuje živé spermie, jsou použity k oplození vajíček metodou ICSI.
V případě, že technikou MESA nebyly získány žádné spermie, přistupujeme k technice TESE. Jde o zákrok, kterým lze získat spermie z kanálků zárodečného epitelu v případě, kdy nejsou schopny uvolnění, či transportu z varlete do nadvarlete.
Z malých řezů v obalu varlete se získá malé množství tkáně varlete. Získaná tkáň je pak dále zpracována v laboratoři. Pokud jsou v embryologické laboratoři nalezeny živé spermie, jsou použity za pomocí metody ICSI k oplození vajíček.Při opakovaně potvrzené azoospermii (žádné živé spermie v ejakulátu) nelze zaručit zisk použitelných spermií výše uvedenými technikami. O výsledku provedené operace je pacient informován ihned po ukončení zákroku.
Klinika reprodukční medicíny a gynekologie Zlín umožňuje svým pacientům využít v rámci léčby neplodnosti moderní metodu kultivace embryí v inkubároru, který je kontinuálně monitorován kamerou. Přístroj EmbryoScope (nebo také embryoskop) je unikátní zařízení, které spojuje do jednoho celku inkubátor, počítač, mikroskop a kamerový systém. Tento specifický inkubátor umožňuje vytvořit ideální podmínky pro růst embrya, které také kontroluje, vyhodnocuje a zaznamenává. Embryologové mají tedy neustálou kontrolu nad tím, v jakých podmínkách se embrya nachází.
Více se o tomto unikátním přístroji se dočtete ZDE.
Proč se používá?
Výzkumy prokázaly, že časné těhotenské ztráty (spontánní potraty, zamlklá těhotenství) a selhání implantace (uhnízdění embrya), které se projevuje neplodností, nebo opakovaným selháním léčby asistovanou reprodukcí, mohou být způsobeny nadměrnou aktivitou NK buněk(„Naturall Killer“). NK buňky jsou specifickou populací bílých krvinek, starající se o obranyschopnost organismu, jejich aktivní forma však může napadnout i embryo, uhnizďující se do děložní dutiny a oslabit ho natolik, že dojde k jeho zániku. Bylo prokázáno, že včasné podání Intralipidu dokáže zabránit aktivaci NK buněk. Bez této aktivace pak NK buňky nepředstavují pro embryo žádné nebezpečí.
Co je to Intralipid?
Intralipid je sterilní tuková emulze, skládající se z frakcionovaného sójového oleje, pomocnými látkami jsou frakcionovaný vaječný lecitin, glycerol, voda pro injekce a hydroxid sodný (pro úpravu pH).
Kdy je nejlepší čas pro aplikaci Intralipidu?
Zhruba týden před přenosem embryí do dělohy, ev. cca 2 dny před ovulací. Hormony produkované po uvolnění vajíčka (progesteron) mají přímý vliv na aktivaci NK buněk. Optimální účinek Intralipidu je tedy možné očekávat, pokud se podá ještě před vzestupem hladiny progesteronu. Na již aktivované NK buňky nemusí být Intralipid účinný.
Jak se intralipid používá?
Intralipid se aplikuje nitrožilně v pomalé infúzi, po zavedení kanyly do předloktí, doba aplikace je cca 90 minut. Během této doby jste pohodlně usazena popř. uložena a jste pod dozorem zdravotnického personálu. I během aplikace můžete normálně jíst a pít.
Jaká jsou rizika použití Intralipidu?
V naprosté většině případů je aplikace snášená naprosto bez obtíží a nevyskytují se žádné závažné vedlejší účinky. Popisované vedlejší účinky jako bolesti hlavy, nevolnosti, třes, zvýšená teplota, jsou velice vzácné a nevyskytují se ani v 1 % případů. Po aplikaci nejsou nutná žádná omezení.
Metoda selekce spermií založená na magnetické aktivaci apoptotických spermií - MACS (Magnetic - Activated Cell Sorting) Systém.
Všechny spermie mají omezenou životnost a zanikají procesem zvaným apoptóza. U spermií, kde už byl proces apoptózy zahájen, je vysoká pravděpodobnost výskytu fragmentací (zlomů) DNA. Tyto zlomy bohužel nelze odhalit pomocí mikroskopu (metody ICSI, PICSI). Pokud jsou apoptotické spermie použity pro oplození vajíčka, tak je vyšší pravděpodobnost, že se embryo z nich vzniklé nebude ideálně vyvíjet, popřípadě se ve vývoji zastaví úplně.
Pomocí MACS jsme schopni magneticky označit apoptotické spermie, které po protečení vzorku speciální kolonou zůstanou zachycené uvnitř, zatímco spermie bez známek apoptózy zachytneme pod kolonou. Tyto „živé" spermie bez známek fragmentace DNA pak můžeme použít pro další metody léčby: IUI, IVF, ICSI, PICSI.
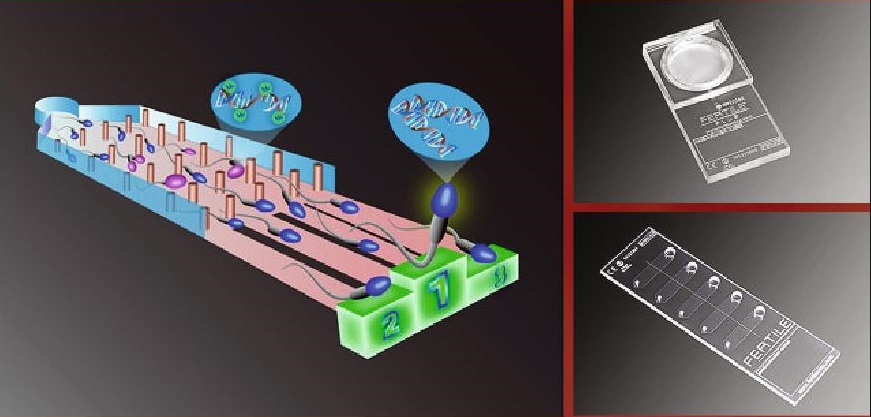
Mikrofluidní čip pro selekci spermií
Tato nová laboratorní metoda selekce spermií používá speciální skleněný čip s mikrobariérami, který třídí spermie na principu přirozeného výběru.
Mikrobariéry napodobují přirozené prostředí vejcovodů ženy.
Vyselektované spermie mají lepší morfologii, životaschopnost a pohyblivost.
Celý proces probíhá bez jakéhokoli přidání dalších chemikálií a zvyšuje úspěšnost cyklu až o 25 %
Předpokladem pro úspěšné oplození vajíček je jejich zralost.
Zralost vajíček je standardně hodnocena embryologem pod světelným mikroskopem. Za zralé se považuje vajíčko s přítomným tzv. polárním tělískem.
Ale ani takové vajíčko nemusí být opravdu zralé. Důležitá je přítomnost dělícího vřetýnka, které je nezbytné pro správné rozdělení chromozomů po oplození. Nyní můžeme dělící vřetýnko neinvazivně detekovat díky nové metodě zobrazení – polarizační mikroskopii a provést oplození (ICSI / PICSI) opravdu zralých vajíček.
Tato metoda je vhodná pro pacientky s nižším počtem získaných oocytů a u pacientek, u kterých došlo k selhání oplození v předchozích IVF cyklech.
PRP terapie (Platelet-Rich Plasma) je inovativní a šetrná metoda, která využívá plazmu získanou z vlastní krve. V té je po zpracování vyšší koncentrace krevních destiček s velkým množstvím růstových faktorů, které pomáhají tělu regenerovat.
Hlavním přínosem PRP terapie je růst děložní sliznice a zlepšení připravenosti dělohy na uhnízdění embrya, protože kvalita sliznice je zásadní pro úspěšné umělé oplodnění.
Pokud děložní sliznice nedosahuje požadovaných parametrů, snižuje se šance na uhnízdění embrya a zvyšuje se riziko spontánního potratu a jiných komplikací.
Velkou výhodou této metody je také její bezpečnost – jde o buňky, které tělo zná, takže se nemusíte obávat nežádoucích reakcí.
JAK PRP FUNGUJE?
- Odběr krve: Nejprve je odebrána krev z žíly v loketní jamce, která se následně zpracuje ve speciálním zařízení.
- Příprava PRP: Z krve se oddělí plazma bohatá na krevní destičky s vysokou koncentrací růstových faktorů, které podporují regeneraci tkání.
- Aplikace: PRP je tenkým katetrem aplikováno do děložní dutiny. Proces zlepšuje její regeneraci.
PRO KOHO JE METODA VHODNÁ?
Metodu doporučujeme ženám, které potřebují zlepšit kvalitu děložní sliznice (např. před transferem embryí).
Výhody PRP
- Bezpečný zákrok, který nevyžaduje invazivní zásahy.
- Pomáhá zvýšit šanci na otěhotnění.
- Použití vlastního biologického materiálu minimalizuje riziko alergických reakcí.
- Podporuje růst a kvalitu děložní sliznice.
JAKÝ JE POSTUP LÉČBY?
- Konzultace: Lékař vyhodnotí situaci a navrhne individuální léčebný plán.
- Aplikace PRP: Proces je rychlý, bezbolestný a obvykle trvá několik hodin.
- IVF cyklus: Aplikace PRP je vhodná na začátku standardního IVF cyklu či KET.

